Celica je osnovni gradnik našega telesa, pa še vedno o njej vemo malo. V njej je kup organelov, na desettisoče različnih proteinov ter drugih akterjev, ki švigajo okoli, vsak s svojo nalogo. Precej huje kot v panju ali ogromnem mravljišču, zato je dogajanju težko slediti, še težje pa ga preučevati. Celica je z informacijskega vidika en velik program z ogromnim številom informacijskih zank, ki jih znanstveniki počasi, počasi razkrivajo.

Vsekakor se vse začne z DNK, molekulo, ki nosi osnovne informacije o vsakem posameznem bitju. Če poenostavimo, DNK je neke vrste knjižnica. Sama po sebi ne počne veliko. Nekdo mora priti in prebrati knjige na policah. To počne neka druga molekula, poimenovana RNK polimeraza, ki igra vlogo "bralca". Specifičen set knjig, ki jim pravimo geni, prebere in sporočila prenese naprej v obliki molekul RNK. Na njihovi podlagi se lahko na koncu sestavijo proteini, ki se odpravijo okrog po celici in počnejo, kar jim je namenjeno. Vse to je zelo, zelo poenostavljeno.
Nov delček v tem kompleksnem dogajanju je uspelo razkriti slovenskemu znanstveniku, ki deluje na Finskem, molekularnemu biologu Matjažu Barboriču. Natančneje, v svojem laboratoriju je skupaj s sodelavci ugotovil, kaj se zgodi, ko je košček DNK poškodovan. Identificiral je mehanizem, ki celici pod genotoksičnim stresom omogoči preživetje. Raziskava, objavljena v znanstveni publikaciji Molecular Cell, nakazuje tudi potencialne poti za zdravljenje raka.
Besedilo raziskave je prosto dostopno na spletni strani laboratorija.
Po sledi pokvarjenih genov
Že ena sama sprememba v DNK je lahko nevarna, je Barborič povedal za MMC. Pokvarjen zapis namreč pripelje do pokvarjenih rezultatov. Ali postane branje nemogoče ali pa celo pripelje do napačno sestavljenega proteina, kar lahko povzroči poškodbe in napake v kompleksnem celičnem dogajanju. Tudi do raka lahko pripelje, če je napaka take vrste, da utiša programirano celično smrt, celico pa zavrti v krog neskončnega deljenja ali pa "večnega" življenja.
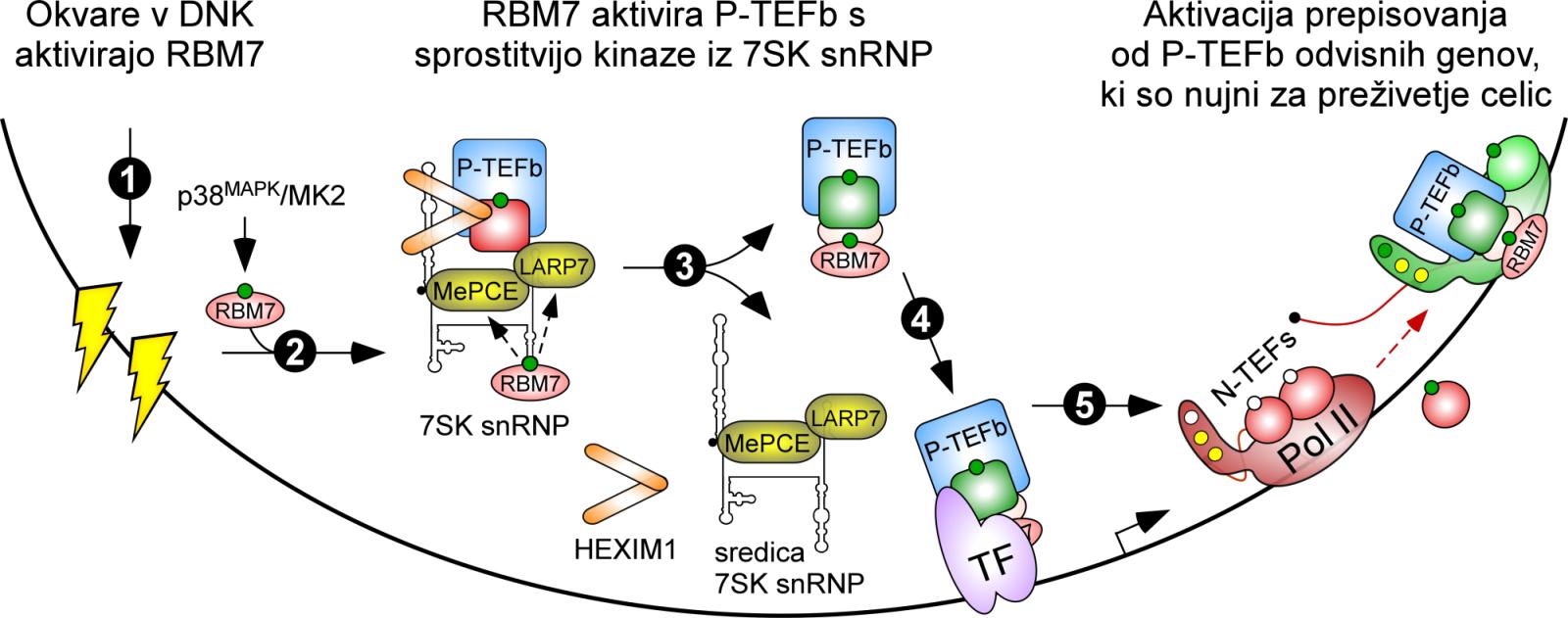
Mutacije v celici lahko privedejo do raka. Celica ima mehanizem, s katerim poskuša preprečiti, da bi do raka prišlo. Mi smo ugotovili, da se po napaki v DNK aktivira signalna pot, kopica proteinskih kinaz, ki pošlje signal do ene majhne molekule z regulatorno vlogo, P-TEFb. In ta molekula je ključna, da se celice odzovejo s prepisovanjem tisočev genov, ki - vsaj po našem modelu - ustavijo celični cikel. To pomeni, da se celica ne deli več naprej in dobi čas, da lahko popravi napake. In ko so popravljene, se ti geni utišajo, celica pa nadaljuje prejšnji program.
Poškodbe DNK med drugim nastanejo pod ultravijoličnimi žarki. Fotoni svetlobe v tem primeru valujejo tako hitro, da prodrejo vanjo in nosijo dovolj energije, da lahko spremenijo kemično sestavo dednine. Doktorski študent Andrii Bugai je v laboratoriju simuliral poškodbo s kemikalijo, ki ima podoben učinek, in opazoval, kako se celica na nezgodo odzove.
Prepisovanje je lahko zelo zapleteno
Prepisovanje nekega tipičnega gena je, spet, zapleten postopek. Izvaja ga RNK polimeraza, ki se plazi po DNK in prepisuje informacije v molekule RNK. Toda narava postopka je taka, da se praktično takoj po začetku branja polimeraza ustavi in čaka v "nizkem štartu". Celica ji mora povedati, ali njeno delo potrebuje ali ne, prek informacijskega mehanizma, ki vsebuje kup različnih molekul z zapletenimi kraticami.
Vse skupaj se navadno konča s kratico P-TEFb. To je protein, sestavljen iz dveh pomembnih delov, poimenovanih CDK9 in CycT. Kot celota P-TEFb deluje kot kinaza, ki pride do RNK polimeraze in ji sporoči, naj nadaljuje branje.
Branje polimeraze se ustavi tudi, ko je na DNK poškodba, ki jo povzročijo fotoni svetlobe ali kemikalija, ki jo je uporabil Bugai. Dva osnovna gradnika se medsebojno povežeta s kovalentno vezjo, kar je narobe. Takrat se sproži nova vrsta domin: genotoksični stres.
Celica uvede izredno stanje
Raziskovalna skupina je ugotovila, da se pod genotoksičnim stresom v celici aktivira protein RBM7, kar privede do njegove vezave na specifično molekulo RNK z imenom 7SK, ki drži že prej omenjene molekule P-TEFb v neaktivnem stanju . (Poprej so znanstveniki mislili, da je RBM7 povezan predvsem z nadzorovanim razkrojem RNK.)
In kaj stori ta RBM7? Prekine povezavo med P-TEFb in 7SK, in tako prebudi molekule P-TEFb, ki skočijo v akcijo in v celici sprožijo "eksplozijo dogajanja". RNK polimeraze iz nizkega štarta na tisoče genov poženejo v branje, kar naposled privede do neke vrste izrednega stanja. Celični cikel se ustavi in s tem celica pridobi čas, da pošlje popravljalne proteine, ki izrežejo poškodovani del DNK ter ga nadomestijo s pravilnim. Če gre vse po sreči, seveda. Lahko tudi ne.

Usodne odločitve
To je usodna točka za malo celico. Ugotoviti in odločiti se mora, ali je dovolj popravljena, da nadaljuje življenje, ali pa prostovoljno izvede "harakiri". Programirano celično smrt, ki ji rečejo tudi apoptoza. Nekatere celice izberejo tudi senescenco, neke vrste neaktivno životarjenje.
Pravzaprav je to lahko tudi usodna točka za celoten organizem. Če napake v DNK niso zadostno popravljene, pa jo celica ubere naprej, lahko postane tudi rakava.
Raziskava je pokazala, da je P-TEFb ključen za preživetje celice. Ko so poškodovani celici zavrli par RBM7-P-TEFb, je šla v pogubo. In ko niso, je celila načeloma popravila poškodbo in se vrnila v stari program. Molekule P-TEFb so se zavile v spanje, RNK polimeraze pa so se na genih, ki so bili ob stresu prepisovani, spet povrnile v nizki štart.
Potencial zdravila za raka
"Vedno bolj postaja znano, da je veliko vrst rakastic celic odvisnih od kinaze P-TEFb," je razkril Barborič. Kako odvisnih? V rakastih celicah delujejo onkogeni, ki so ključni za preobrazbo iz normalnih celic v abnormalne. Onkogeni povzročajo celici stres, ki je podoben prej opisanemu genotoksičnemu. "Tega sicer še nismo dokazali, ampak to je zdaj nadaljevanje zgodbe," je poudaril sogovornik.
"Ključna stvar pri raku je, da se skozi njegovo evolucijo ustvarijo napake, pri katerih se začnejo celice naenkrat nebrzdano množiti. In tedaj potrebujejo to našo kinazo P-TEFb, saj prepisuje določene proteine, ki preprečujejo celično smrt."
Poenostavljeno, te rakaste celice si ustvarjajo stres, da lahko živijo "večno" in se nebrzdano razmnožujejo. Za to je nujen P-TEFb.
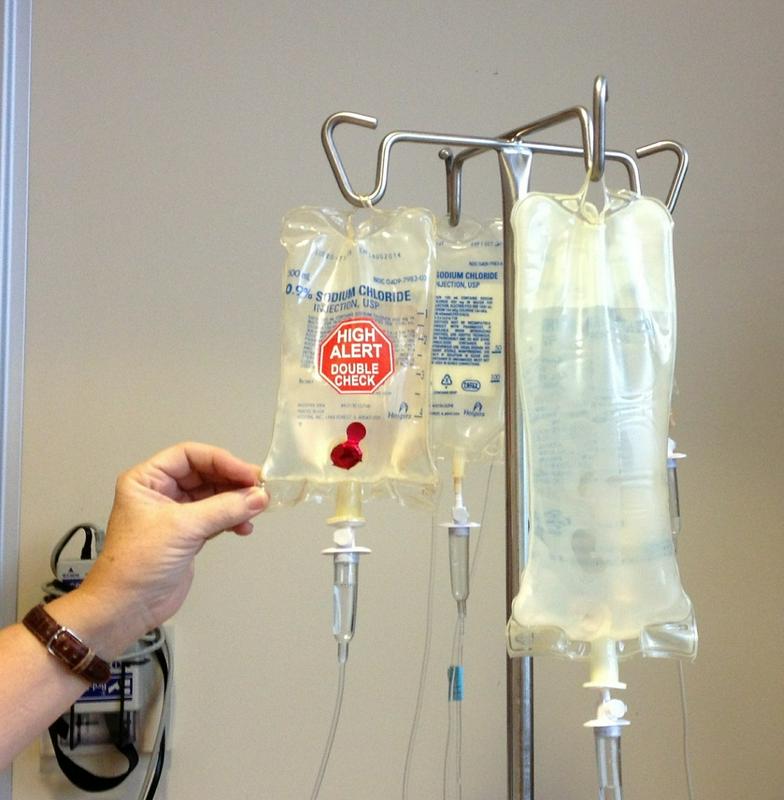
Zahtevno uravnavanje kemoterapije
Logika izriše tudi obraten scenarij. Če se v rakasto celico vnese inhibitor kinaze, celica odmre, sproži se apoptotična smrt. "To je zdaj še malce špekulativno. Nadaljujemo delo in imamo zelo dobre rezultate, ampak delo še ni objavljeno," je dodal biolog.
Da so nekatere rakaste celice odvisne od kinaze, je že bilo znano. Ni pa bilo čisto jasno, zakaj. "Naš mehanizem razloži vsaj del zgodbe."
Mehanizem, ki se lahko uporabi pri kemoterapiji. "Veliko danes obstoječih kemoterapij uporablja kemikalije, zelo podobne tistim, ki smo jih mi uporabljali, ki torej kvarijo DNK. Če bi istočasno vnesli še inhibitorje P-TEFb, bi zagotovo veliko bolje delovala."
Problem je "samo", kako bi inhibitor deloval na človeško telo kot celoto. "Vprašanje je, ali bodo vse celice umrle. Če v rakaste vneseš inhibitor, potem ni beljakovin, ki bi preprečevale celično smrt, zato odmrejo. Kaj pa bo z zdravimi celicami?" je opozoril.
Scenarij ni nujno črn, saj kot rečeno, rakaste celice kinazo nujno potrebujejo, medtem ko jo zdrave precej manj, in bi morebitna nizka koncentracija inhibitorja zadostovala, da bi odmirale le rakaste. Še najlažje bi bilo, če bi našli način za vnos zdravila samo v rakaste celice ali v omejeno okolico tumorja.
Klinične študije so v teku, je dodal Barborič.
Zdaj gremo vedno bolj v to, da bi ugotovitve nekako uporabili v terapevtske namene. Toda osnova so vedno bazične raziskave. Brez tega ni nobene terapije, in zato je zelo važno, da države osnovne raziskave podpirajo. V to Finska precej vlaga.
20 let znanosti v tujini
Barborič je večino svojih znanstvenih let preživel v tujini. Kot mikrobiolog je diplomiral na Univerzi v Ljubljani in se kaj kmalu zatem znašel v San Franciscu. "V času opravljanja diplomske naloge sem poslušal predavanje Matije Peterlina. Imel ga je na Institutu Jožef Stefan (IJS), ki ga je ustanovil njegov oče. Zelo me je navdušil, ko je govoril o virusu HIV in kako s pomočjo proteinov človeških celic prepisujejo svoj dedni zapis. Stopil sem do njega, mu dejal, da me zanima njegovo delo, in čez nekaj mesecev sem že eksperimentiral v njegovem laboratoriju na kalifornijski univerzi v San Franciscu," je opisal. Tam je končal doktorat, pa še podoktorsko šolanje. Po desetih letih se je preselil na Univerzo v Helsinkih, kjer je dobil denar za ustanovitev lastnega laboratorija, ki ga vodi še danes.

Finsko življenje
Kakšno je pa kaj življenje na Finskem? "Življenje je preprosto. Finci so v osnovi nezahtevna skupnost, ki je skromnost revnega življenja iz preteklosti ohranila do današnjih dni," je opisal. "Stopiš v povprečno trgovino in je kot bi vstopil v trgovino v Sloveniji pred 30 leti. Ni kupa istih izdelkov, ki se razlikujejo le po barvi."
Po njegovih besedah na Finskem stopnja neenakosti ni visoka, je pa močan socialni čut za sočloveka. "Držijo drug z drugim, ker se zavedajo, da smo vsi na isti ladji."
Ljudem je poleg dela pomemben tudi prosti čas. Veliko je društev, vsak se z nečim ukvarja, igra kak instrument, pleše, in poleg dela tudi normalno živi. "Kakovost življenja je zato toliko višja," je opisal Barborič, ki z zadovoljstvom uporablja tamkajšnje proge za smučarski tek, saj jih je na tisoče. Pogreša pa smučišča, kot jih najdemo v Sloveniji.





















































 2. sv
2. sv














Komentarji so trenutno privzeto izklopljeni. V nastavitvah si jih lahko omogočite. Za prikaz možnosti nastavitev kliknite na ikono vašega profila v zgornjem desnem kotu zaslona.
Prikaži komentarje