Tretji del serije CEPIVA IN MI.
Skozi tri klinične stopnje
"Na prvi klinični stopnji se v preizkušanju cepiva na ljudeh raziskovalci osredotočajo predvsem na varnost, ob tem spremljajo morebitne neželene učinke na organizmu," pojasnjuje dr. Tomaž Bratkovič, predstojnik Katedre za farmacevtsko biologijo na Fakulteti za farmacijo v Ljubljani. "Najprej cepivo prejme samo eden ali dva udeleženca, nato ju spremljajo nekaj dni, in če ni kakšnih hudih učinkov, je smiselno vključiti tudi nadaljnje prostovoljce, ki so praviloma mladi in zdravi. Pri tem spremljajo reaktogenost oziroma ali na mestu vnosa nastane rdečina oziroma bolečina, ali posameznik dobi vročino, poroča o bolečinah v mišicah … To je pričakovana aktivacija imunskega odziva, ki pa mora biti zmerna in mora izzveneti. Spremljajo tudi imunogenost, pri čemer opazujejo, ali cepivo sproži nastajanje protiteles in aktivacijo limfocitov T."
Če se cepivo izkaže za varno na prvi stopnji, sledi naslednja. Kandidatnih cepiv je nekaj manj, odpadejo ali opešajo prva manj varna ali nezadostno imunogena. Na novi stopnji mora cepivo prestati srečanje s še več prostovoljci. "Na drugi stopnji bodo nekoliko razširili skupino prostovoljcev, ta ne bo več tako izrazito homogena. Smiselno je tudi preveriti, kakšen odmerek bo treba aplicirati." Tako je v primeru cepiv proti covidu-19 v večini primerov že jasno, da ga bo treba odmerjati v dveh odmerkih z različnim časovnim razponom, kar nekaj nezaupanja pa je sprožil nedavni spodrs pri kandidatnem cepivu AstraZenece, kjer še vedno ni povsem jasno, kolikšen odmerek ima najvišjo učinkovitost.

Na tretji klinični stopnji morajo cepivo preizkusiti na več deset tisoč prostovoljcih, v njej spremljajo, ali zmore učinkovito in varno zaščititi ljudi. Ta stopnja je po besedah Bratkoviča "najbolj zapletena, tudi finančno najzahtevnejša. V raziskavo so vključene zelo heterogene skupine ljudi, poleg mladih tudi starejši, kronični bolniki, otroci … pri katerih poleg vseh morebitnih neželenih učinkov spremljajo tudi učinkovitost cepiva." Na tej stopnji del prostovoljcev prejme testno cepivo, del pa placebo, študije so dvojno slepe, kar pomeni, da niti prostovoljci, udeleženi v raziskavi, niti zdravstveno osebje, ki izvaja cepljenje, ne vedo, kaj je udeleženec prejel. Prostovoljce nato spremljajo več mesecev, ti živijo svojo običajno življenjsko rutino in pri tem prihajajo tudi v stik s povzročiteljem bolezni. "Tukaj lahko primerjamo, ali cepivo ponuja zadostno zaščito proti povzročitelju bolezni. Primerjajo namreč obolevnost med obema skupinama in statistična analiza pojavnosti bolezni med cepljenimi in tistimi, ki so prejeli placebo, bo dala informacijo, ali je cepivo zares učinkovito."
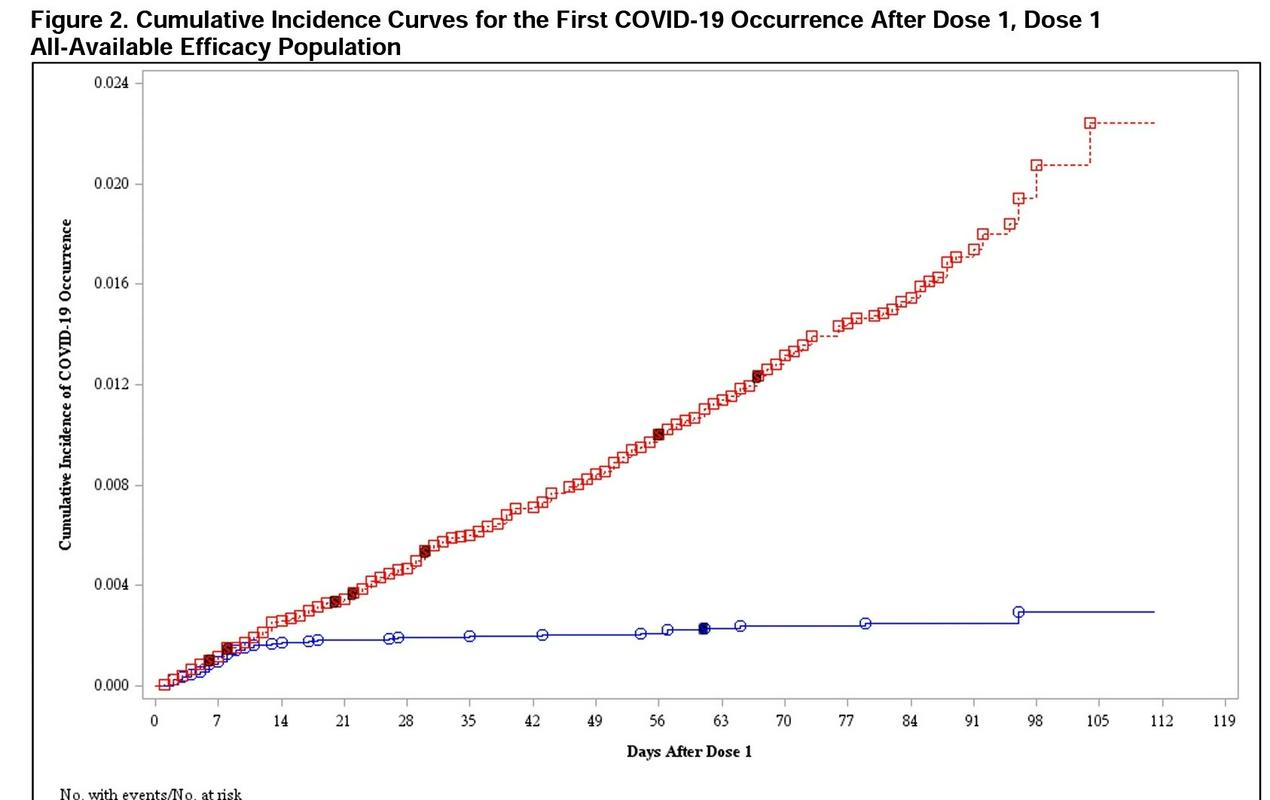
V zadnjih tednih je nekaj proizvajalcev poročalo o izjemno visoki, več kot 90-odstotni učinkovitosti njihovega kandidata, kar je tudi dr. Roman Jerala, vodja Odseka za sintezno biologijo in imunologijo na Kemijskem inštitutu, pospremil z odobravanjem: "To je zelo opogumljajoča informacija. Cepivo je preprečilo bolezen v precejšnjem deležu okuženih, številke so zelo visoke, kar je spodbudno. Meja, da bi moralo biti 50-odstotno učinkovito, kar bi bilo primerljivo s cepivom za gripo, je močno presežena." Toda pri tem je po njegovih besedah treba vzeti na znanje tudi, da se več kot 90-odstotna učinkovitost, o kateri poročajo proizvajalci, nanaša na obdobje takoj po končanem cepljenju, ko je imunski odziv na vrhuncu. "Vemo, da titer protiteles precej upade, a upam, da končna zaščita ne bo veliko slabša. Še vedno pa je to dober obet." S prvimi uspešnimi kandidati so po njegovem tudi dokazali, da je bila usmeritev v snovanje cepiva na podlagi virusnega S-proteina, torej virusne konice, dobra. "To obeta, da bodo ostala cepiva prav tako uspešna."
Tokrat bliskovit razvoj pospešil … denar
Varnost je nekaj, pri čemer se ne sme prehitevati in pri čemer se tudi ni prehitevalo. Preverjanje varnosti teče kot običajno. Čeprav prvi stopnji skoraj takoj sledi druga, ljudem, ki so bili vključeni vanjo, še vedno sledijo dve leti, kot je to običajno.
Normalno za razvoj posameznega cepiva preteče tudi desetletje ali desetletje in pol. Kako je torej mogoče, da so se tokrat stvari tako drastično pospešile? Dr. Florian Krammer. profesor vakcionologije na newyorški šoli medicine Icahn Mount Sinai, ki je nedavno v reviji Nature objavil tudi pregleden članek o ključnih kandidatih, se sklicuje predvsem na denar. "Res je, običajno traja približno 15 let, da razvijete cepivo, včasih tudi dlje. Ključno zavoro pri tem predstavlja pomanjkanje sredstev. Pri vsaki novi stopnji je treba na novo utemeljevati, ali sta razvoj in izdelava cepiva še smiselna, dokazovati je treba, ali je cepivo res tako kakovostno. Vlagatelji preračunavajo, kako dobičkonosno bo cepivo in ali se izplača tvegati … Ta hip teh pomislekov ni. Denarja je na pretek, zato lahko razvoj cepiva napreduje tako hitro." Zaradi specifičnih okoliščin je mogoče postopek po njegovih besedah na določenih točkah tudi občutno skrajšati. "A varnost je nekaj, pri čemer se ne sme prehitevati in pri čemer se tudi ni prehitevalo. Preverjanje varnosti teče kot običajno. Čeprav prvi stopnji skoraj takoj sledi druga, ljudem, ki so bili vključeni vanjo, še vedno sledijo dve leti, kot je to običajno." To, da je tokrat razvoj cepiva tako pospešen, je torej po njegovem odvisno od dveh dejavnikov: prvič, imamo vse bolj izpopolnjeno tehnologijo, in drugič, na voljo je skoraj neomejeno finančnih sredstev. "A še enkrat, bližnjic na področju preverjanja varnosti ni."
Zapleti pri kliničnih stopnjah lahko tudi končajo razvoj cepiva
Pri tem se zastavlja vprašanje, kolikšna je v testnih kliničnih stopnjah še sprejemljiva stopnja neželenih učinkov. "Vedno je treba pretehtati korist za splošno populacijo in pa s tem povezano tveganje za posameznika," razlaga Tomaž Bratkovič. "Vemo, da absolutno varnih cepiv in zdravil ni, neželeni učinki so vedno mogoči. Pri tem pa je pomembno, da cepivo tudi po pridobitvi dovoljenja za promet podrobno spremljajo še naprej." Pri tem je pod drobnogledom varnost, zapisujejo se vsakršni neželeni učinki. Če se kdaj pozneje izkaže, da so neželeni učinki resni in da so jih v kliničnem vrednotenju spregledali ali nanje niso naleteli, je to lahko razlog za odpoklic. Takšno je bilo živo oslabljeno cepivo pri otroški paralizi, ki lahko pri enem od dveh milijonov in pol prejemnikov povzroči reaktivacijo sicer oslabljenega virusa, ki izzove bolezen, čeprav bi jo moral preprečiti, navaja Bratkovič. Številne države so se tudi zato raje odločile za milejšo različico inaktiviranega cepiva.
Kot smo se lahko prepričali tudi pri razvoju aktualnega cepiva, ki ga snuje AstraZeneca, lahko en nejasen primer hudih neželenih učinkov postopek ustavi, stvar se razišče, skuša se dognati, ali je dogodek povezan s cepivom. To izvede neodvisen odbor strokovnjakov in šele na podlagi njihove odločitve se lahko začasno prekinjena klinična stopnja nadaljuje.
Po besedah Floriana Krammerja sicer "ni videti, da bi bila smrt udeleženca v tej raziskavi povezana s cepivom, sicer klinične stopnje ne bi nadaljevali. Kot ste najbrž prebrali v medijih, naj bi eden od udeležencev zbolel za transverzno mielopatijo oziroma vnetjem hrbtenjače. A naj spomnim, da je za podobnim zapletom trpel tudi eden od udeležencev tretje stopnje testiranja cepiva proti HPV, ki je pozneje kljub temu dobilo licenco. Takšne stvari zahtevajo previdnost. Če cepite 30.000 ljudi, obstaja verjetnost, da bo kateri od njih huje zbolel ali celo umrl. A ne zaradi cepljenja, ampak ker je verjetnost, da se kaj takega zgodi, v tako številni skupini visoka. In najverjetneje se je nekaj takega zgodilo tudi pri testiranju cepiva AstraZenece, najverjetneje pa zaplet ni povezan s cepivom." "Ni podatka, ali je hujši zaplet nastal pri nekom, ki je prejel kandidatno cepivo ali placebo, ti podatki so za zdaj slepi," je pripomnil tudi Tomaž Bratkovič. "Je pa tako, da se lahko pri preverjanju cepiva na 30.000 prostovoljcih zgodijo tudi nepričakovani zapleti, celo smrti, ki niso nujno vzročno povezani s cepljenjem. Lahko da katerega od teh zbije avto, pa vzrok za to težko pripišemo cepivu."
Je pa tako, da se lahko pri preverjanju cepiva na 30.000 prostovoljcih zgodijo tudi nepričakovani zapleti, celo smrti, ki niso nujno vzročno povezani s cepljenjem. Lahko da katerega od teh zbije avto, pa vzrok za to težko pripišemo cepivu.
Postopek registracije v ZDA drugačen kot v Evropi
Regulatorni organi bodo vse rezultate predkliničnih in kliničnih raziskav temeljito pregledali, strne Bratkovič. Ti organi po njegovih besedah delujejo neodvisno, prihajajo iz različnih držav. Po preverjanju dokumentacije lahko izdajo pozitivno ali pa odklonilno mnenje, po potrebi lahko zahtevajo tudi dodatne raziskave. Po izdaji pozitivnega mnenja sledi tudi izdaja dovoljenja za prodajo cepiva. Celotna razvoj in potek raziskav sta po njegovih besedah izjemno draga. "Stroški se lahko dvignejo tudi do dveh milijard ameriških dolarjev. Torej ni presenetljivo, da so se le večji igralci, ki že imajo izkušnje z razvojem cepiv, vključili v aktualno tekmo za cepivo."
Združene države in Evropska unija sicer po Krammerjevih besedah ubirajo vsaka svojo pot pri podeljevanju licence. "V ZDA gre cepivo skozi redni postopek, ki sicer traja nekaj časa, v postopku pridobivanja pa dobiš dovoljenje tudi za izredno uporabo cepiva še pred pridobitvijo uradne licence. Tak način postopka smo pričakovali tudi v tem primeru, a težava pri uveljavljanju izredne uporabe cepiva za nujne primere je, da moraš cepiti tudi vse tiste, ki so bili v skupini s placebom, tu pa zna nastati težava. Skupina je po eni strani namreč še vedno del tretje stopnje klinične študije, a če jo cepiš s pravim cepivom, ta del raziskave izgubi smisel. Tako ta hip potekajo pogajanja, kako bi lahko našli primerno rešitev za to, da bi bilo cepivo čim prej na voljo in da se ne bi izgubili ključni podatki v poteku raziskave." Tudi v Evropi po njegovih besedah obstajata dva načina pridobitve licence, eden je prav tako pospešen kot v ZDA, a obstajajo razlike. "V ZDA zbereš vse podatke, in ko meniš, da jih imaš dovolj za pridobitev licence, vse skupaj predaš Agenciji za zdravila. V Evropi je vse skupaj podobno postopnemu dialogu z Evropsko agencijo za zdravila. Rezultate raziskave agenciji oddajaš sproti, in ko se ta nekega dne odloči, da ima dovolj podatkov, presodi o primernosti kandidata. S tega stališča je postopek v Evropi malo manj predvidljiv, saj ni postavljenih natančnih časovnih rokov."
Evropska agencija za zdravila o registraciji cepiv v Evropi
Po Krammerjevih besedah so sicer v primeru cepiva proti covidu-19 v tretji klinični stopnji zelo raznovrstni kandidati. "Če spodleti eni tehnologiji, lahko upe usmerimo v drugo, čeprav sam menim, da na tej točki najbrž ne bo spodletelo nobenemu izmed kandidatov, ki so že na tretji stopnji."
Kaj pa kitajski in ruski kandidati?
Med cepivi obstaja razlika. Kot pojasnjuje Florian Krammer, imamo na eni strani cepiva, ki jih razvijajo na Kitajskem, "in zelo malo možnosti je, da bi ta cepiva v prihodnje uporabljali v Severni Ameriki ali v Evropi. In na drugi strani so tu cepiva, ki jih razvijajo v Ameriki in Evropi. Kitajska se precej osredotoča na razvoj inaktiviranega tipa cepiv, ta hip so na tretji klinični stopnji kar tri takšna cepiva, ki jih pripravljajo, na zelo napredni stopnji je tudi cepivo na podlagi adenovirusov. Imamo tudi rusko cepivo, ki je prav tako utemeljeno na podlagi virusnih vektorjev, a je zelo malo verjetno, da bi ga za uporabo registrirali v Evropi ali Ameriki." Cepiva, ki so ta hip najdlje v razvoju v Evropi ali Ameriki, po večini temeljijo na RNK- ali virusnih vektorjih, po Krammerjevo obetajo tudi kandidati na podlagi rekombinantnega proteina.
V Veliki Britaniji so zdaj prvi v Evropi že odobrili cepivo proti covidu in začeli cepiti. Tamkajšnji regulator MHRA je v začetku meseca sporočil, da je cepivo, ki nudi do 95-odstotno zaščito pred boleznijo covid-19, varno in se lahko začne uporabljati. Tudi svetovalni odbor ameriške Uprave za hrano in zdravila je v četrtek priporočil izdajo izrednega dovoljenja za uporabo cepiva podjetij Pfizer in BioNTech v Združenih državah Amerike, prihodnji teden pa bo odbor odločal o cepivu podjetja Moderna. Prvi Američani naj bi bili cepljeni v ponedeljek ali torek. Pfizerjevo cepivo so sicer doslej odobrili tudi v Kanadi, Bahrajnu in v Savdski Arabiji. "Tudi Rusija je sicer svojemu kandidatu že podelila licenco, a ne gre za licenco v pravem pomenu besede. Tudi sami so ta hip še na tretji stopnji, tudi oni čakajo na dejanske rezultate, ali je cepivo res varno in učinkovito. Nekaj podobnega je storila tudi Kitajska, ki je eno od cepiv, ki je prav tako na tretji stopnji, že uporabila na pripadnikih svoje vojske. To je sicer precej pogosta praksa. Tudi v ameriški vojski so v uporabi določene vrste cepiv, ki sicer še niso bila odobrena za uporabo na širši populaciji."
Metaštudij med posameznimi kandidati proti covidu-19 za zdaj še ni
Bratkovič je sicer ob tem izrazil obžalovanje, da ne obstaja nobena mednarodna metaštudija, ki bi primerjala učinkovitost najobetavnejših kandidatov med cepivi proti covidu-19. Kot je k temu pripomnil Krammer, so sicer študije na nečloveških primatih pokazale na določene razlike v nastajanju ustreznih protiteles in zaščite (nekatera so boljša pri zaščiti zgornjega dela dihalnega trakta kot druga), so pa doslej vsi najnaprednejši kandidati dobro zaščitili spodnji del dihal. "Hipna primerjava je težavna, saj cepiv ne dovajajo v enakih odmerkih, do primerjave pa moramo biti kritični. Na ravni človeških raziskav obstaja nekaj iniciativ (CEPI, WHO), da bi medsebojno primerjali imunološke podatke na ravni titrov, protiteles in tako naprej. Opravljena tretja stopnja bo vsekakor ponudila možnosti za takšne razširjene primerjalne študije."
Priprava milijard odmerkov cepiva ne bo mačji kašelj
Medtem ko najuspešnejša kandidatna cepiva čakajo na odločitve regulatornih organov, se zastavlja vprašanje, kako v kratkem času zagotoviti zadostno proizvodnjo cepiv. Takoj ko cepiva prejmejo tržno dovoljenje, bodo lahko na voljo za uporabo na trgu, zato se družbe po večini že pred pridobitvijo dovoljenja odločajo za vnaprejšnjo proizvodnjo na zalogo.
Da bi širjenje virusa po svetu lahko zajezili, je treba doseči zadostno precepljenost v celotni svetovni populaciji. Ker bosta pri večini cepiv potrebna dva odmerka, bo treba v kratkem času izdelati več milijard odmerkov cepiva. To lahko predstavlja težavo, opozarja dr. Aleš Berlec z Odseka za biotehnologijo na Inštitutu Jožefa Stefana. "Rešitev ni tako preprosta, da bi samo povečali prostornino posode za proizvodnjo cepiva. Obstaja več dejavnikov in ravno zato so se proizvajalci cepiv povezali z večjimi farmacevtskimi podjetji, ki lahko zagotavljajo ustrezne kapacitete. Govorim o proizvodnih obratih oziroma tovarnah, ki lahko proizvedejo velike količine cepiv, zagotavljajo potrebno infrastrukturo, upravljajo odpad, ki pri tem nastane. Vse to je v kratkem času težko postaviti na novo, zato družbe uporabljajo partnerje, farmacevtsko industrijo, ki že ima ustrezne izkušnje in kapacitete."
Ob varnosti in učinkovitosti steber kakovostnih cepiv tudi dobra proizvodna praksa
Prostore, kjer proizvajajo cepiva, si lahko po Berlečevih besedah predstavljamo kot izjemno čiste, sterilne, higiena je na prvem mestu, aparature upravljajo ljudje v zaščitni opremi, vse zato, da se prepreči kakršna koli kontaminacija proizvedenega cepiva. Naš sogovornik pravi, da ne pozna primera, pri katerem bi bil prav produkcijski postopek v farmacevtski industriji kriv za kakršne koli neželene učinke pri prejemnikih cepiv. Razlog je v dobri proizvodni praksi oziroma v izjemno strogih farmacevtskih standardih, ki usmerjajo proizvodnjo cepiva. "V ozadju je veliko regulatornih predpisov, treba je zagotoviti ustrezno vodenje dokumentacije, sledljivost, standardizacijo vhodnih surovin, vse to prispeva h končnemu izdelku zahtevane kakovosti."
Proizvodnjo katerega koli biološkega zdravila, kamor spadajo tudi cepiva, lahko po njegovem razdelimo na dve stopnji: pridobivanje surovine in čiščenje. "V prvem delu gre za pridobivanje, za tako imenovani 'up-stream', gojenje celic, postopke v bioreaktorjih, v katerih pridobijo zadostno količino cepiva. Pri čiščenju cepiva pa je treba tega nato izolirati iz nastale kompleksne mešanice. Pri tem uporabljajo kromatografske tehnike, centrifugiranje, filtracijo in tako naprej, ki omogočajo ločevanje komponent cepiva od drugih snovi, udeleženih v bioprocesu."
Tudi RNK-cepiva so po njegovih besedah še vedno biološka zdravila, čeprav niso proizvedena neposredno v živih celicah. Kot je pojasnil, gre pri proizvodnji mRNK za prepisovanje (strokovno transkripcijo) mRNK iz molekule DNK. Za to potrebujejo molekulo DNK (krožna oziroma tako imenovana plazmidna DNK, ki jo izolirajo iz bakterij Escherichia coli in, zelo poenostavljeno, zmes encimov, ki pospešijo reakcijo. "Ne gre torej za kemijsko sintezo v klasičnem pomenu."

Transport in hramba cepiv mRNA bosta poseben zalogaj
Kot kaže zdaj, naj bi na tržišče najprej prišla platforma cepiv mRNK (uradno se je je oprijelo ime platforma mRNA), ki deluje na podlagi RNK. Kandidatni cepivi farmacevtskih družb Pfizer in Moderna sta te vrste, a bo treba do njiju po Berlečevih besedah pristopati v rokavicah. "Pri takšni platformi je razvoj cepiva vsaj na začetni stopnji lahko bistveno hitrejši. Proizvajalci že imajo na voljo znanje, kako pripraviti molekulo RNK, ta se vede tudi dokaj predvidljivo. Je pa res, da je zaradi svojih lastnosti to zelo občutljiva in nestabilna molekula, ki se lahko hitro razgradi. Prav tako ni izkušenj s proizvodnjo te vrste cepiva." Cepiva na podlagi RNK zahtevajo zelo nizko temperaturo hranjenja, Pfizerjevo celo minus 80 stopinj Celzija. Cepivo bo moralo torej iz proizvodnje do nas potovati pod zelo strogimi in zahtevnimi pogoji, čemur pravimo hladna veriga. "To predstavlja precejšnjo omejitev. Da se zagotavlja taka temperatura ves čas transporta, bodo potrebni posebni vsebniki, uporaba tekočega dušika in suhega ledu, a tudi tu so omejitve. Na letalo gre lahko samo določena količina suhega ledu. Ob vsem skupaj pa bo treba zagotoviti tudi druge surovine za pripravo formulacij, kot je zadostno število steklenih vijal, brizg, tudi o vsem tem mora nekdo razmišljati."
Proizvajalci v razvoju cepiva pred registracijo običajno izvedejo tudi tako imenovane stabilnostne študije. Ob dolgotrajnih, ki lahko trajajo leta, obstajajo tudi pospešene stabilnostne študije. To pot so proizvajalci zaradi časovnih ovir že od začetka postavili strožje pogoje pri proizvodnji in transportu cepiva. Z nabiranjem izkušenj jih bodo vmes najverjetneje še spreminjali in prilagajali.
To predstavlja precejšnjo omejitev. Da se zagotavlja tako temperaturo ves čas transporta, bodo potrebni posebni vsebniki, uporaba tekočega dušika in suhega ledu, a tudi tu so omejitve. Na letalo gre lahko samo določena količina suhega ledu.
Brez svetovne precepljenosti pandemiji ne bomo kos
Kljub zelo dobrim novicam o nekaterih primernih kandidatih za cepivo proti covidu-19 pa se zastavlja vprašanje, ali bodo do njih lahko dostopale izključno države, ki jih izdelujejo? Če dostop do cepiva ne bo omogočen globalno in enakovredno, v boju z virusom ne bomo uspešni.
Proizvajalci cepiv, ki ta hip poročajo o najobetavnejših rezultatih na tretji klinični stopnji, ocenjujejo, da bi lahko do konca prihodnjega leta priskrbeli dovolj odmerkov za cepljenje tretjine svetovnega prebivalstva. Podjetja AstraZeneca, Pfizer in Moderna za prihodnje leto tako napovedujejo proizvodnjo skupno 5,3 milijarde odmerkov, kar bi bilo dovolj za nekaj manj kot tri milijarde ljudi. Dodatne pol milijarde napovedujejo v Rusiji za njihovo cepivo. Večina tega so si že rezervirale najbogatejše države, med njimi evropska sedemindvajseterica in pet drugih najbogatejših držav sveta, ki sicer skupno predstavljajo le 13 odstotkov svetovne populacije. Doslej si je največ odmerkov cepiva na prebivalca – kar devet – rezervirala Kanada, v Evropski uniji pa je ta delež trikrat manjši. Zelo velik delež cepiv si je izborila tudi Indija, kar dve milijardi, kar ni nepričakovano, saj tam deluje največji svetovni proizvajalec cepiv, Serum Institute of India. Pretežni del revnejših držav po svetu je tako potisnjenih v negotovost, da bi se lahko do cepiva dokopale šele po letu 2023.
Prav v ta namen so na svetovni ravni ustanovili posebno pobudo COVAX, ki deluje kot platforma za podporo raziskavam, razvoju in proizvodnji kandidatov za cepivo proti covidu in naj bi zagotavljala njihovo dostavo v države z nižjimi prihodki. Kot so nam pojasnili pri enem od partnerjev pri pobudi, globalnem javno-zasebnem zdravstvenem partnerstvu Gavi s sedežem v Švici, bi imela večina držav, od najbogatejših do najrevnejših, brez COVAX-a le malo upanja za hiter dostop do varnega in učinkovitega cepiva proti covidu-19, ko bo to na voljo. "Izogniti se moramo ponovitvi scenarija, kot smo ga videli v primeru virusa H1N1 in ki je povzročil pandemijo prašičje gripe v letu 2009." Tedaj je nekaj bogatih držav rezerviralo celotno svetovno ponudbo cepiva, velika večina pa je ostala brez dostopa. "Enakovreden svetovni dostop do cepiva, zlasti za zaščito zdravstvenih delavcev in tistih, ki so najbolj ogroženi – ne glede na njihovo lokacijo in finančno stanje, je edini način za ublažitev zdravstvenega in ekonomskega vpliva pandemije na posameznike, skupnosti in narode," poudarjajo v Gaviju. V resnici bomo po njihovem potrebovali vrsto varnih in učinkovitih cepiv, če želimo do konca leta 2021 končati akutno stopnjo pandemije.
Ta hip je v pobudo vključenih 189 gospodarstev, ki predstavljajo večino svetovnega prebivalstva. Med podpisnicami pobude, pomenljivo, ni Združenih držav Amerike, ji pa prek krovne Evropske unije prisostvuje tudi Slovenija. Vsa sodelujoča gospodarstva bodo imela – ne glede na raven dohodka – enak dostop do teh cepiv, ko jih bo skupaj s Svetovno zdravstveno organizacijo razvil in predhodno odobril pristojen regulatorni organ. Sedemindevetdeset gospodarstev z višjimi dohodki se je prijavilo in odobrilo vnaprejšnja plačila, 92 pa jih je upravičenih do podpore iz vnaprejšnje tržne zaveze (angl. Advance Market Commitment oz. AMC).
Iz partnerstva Gavi, ki si je v preteklosti med drugim prizadevalo za izkoreninjenje ebole v Afriki, so ob tem na naša vprašanja pripisali še, da je "cilj pobude COVAX končati akutno stopnjo pandemije do konca leta 2021 z nabavo dveh milijard odmerkov varnih in učinkovitih cepiv proti covidu-19 za najbolj ogroženo populacijo povsod po svetu". Cepiva bodo po njihovih besedah razdeljena takoj, ko se izkažejo za učinkovita, pridobijo regulatorno odobritev in bodo na voljo v ustreznih odmerkih. "Gavi se bo najprej osredotočil na zagotavljanje zadostne oskrbe in virov, da bo vsem sodelujočim gospodarstvom (z nizkim, srednjim in visokim dohodkom) zagotovil cepiva za načrtovano cepljenje petine prebivalstva, tu bo šlo predvsem za zdravstvene in socialne delavce, starejše in tiste z obstoječimi kroničnimi boleznimi. Iščemo tudi načine, kako bi lahko revnejšim državam še povečali količino odmerkov ob podpori Svetovne banke in drugih regionalnih razvojnih bank."
Kaj pa kakovost cepiv, ki potujejo v tretje države?
Revnejše države si praviloma težje privoščijo dostop do cepiv, zato potrebujejo izdatno mednarodno pomoč. Kakšne so ob tem možnosti, da zaradi šibkejšega finančnega položaja posegajo po manj kakovostnih, celo testnih cepivih? Infektolog in pediater dr. Marko Pokorn z ljubljanske Pediatrične klinike je pri tem spomnil na misel očeta sodobne vakcinologije Stanleyja Plotkina, sicer ključnega snovalca cepiva proti rdečkam. Plotkin je med drugim trdil, da denar nima nič s tem, kar je v brizgi. "Cepiva, ki se uporabljajo po svetu, so enake kakovosti. Ob tem je treba omeniti, da nekatere države tretjega sveta, denimo Indija, proizvajajo tudi svoja lastna cepiva, ki so učinkovita in varna in jih lahko sami proizvajajo v velikih količinah." Na splošno je dostopnost cepiv proti najhujšim boleznim po svetu dobra, poudari. "Za to si prizadeva tako Svetovna zdravstvena organizacija kot tudi nekatere druge organizacije, svetovne iniciative za eradikacijo določenih bolezni. Ena takih je tudi fundacija Billa in Melinde Gates, ki zagotavlja cepiva tudi v državah, ki si tega ne morejo privoščiti."
Malarija ostaja težak izziv
Prav države v razvoju sicer še naprej opozarjajo na ključne izzive pravičnega vsestranskega dostopa do cepljenja. Med drugim se porajajo kritike, da bi se lahko svet učinkoviteje spopadal s smrtonosnimi epidemijami, ki razsajajo zlasti v državah tretjega sveta, če bi se jim odmerjala podobna politična in finančna pozornost kot covidu-19. Ena takih je tuberkuloza, ki naj bi skupno v zgodovini zahtevala do milijarde in pol življenj, prav tako še vedno čakamo na učinkovito cepivo proti malariji. Zaradi malarije letno zboli 200 milijonov ljudi, približno 400.000 jih bolezni podleže, od tega je 80 odstotkov otrok, mlajših od pet let.
K bolj zavzetemu in vzajemnemu svetovnemu ravnanju v boju proti malariji je v aktualnem poročilu 30. novembra pozvala tudi Svetovna zdravstvena organizacija. Od podpisa posebne deklaracije o preprečevanju malarije leta 2000 v Abudži naj bi jim sicer v Afriki, kjer potrdijo kar 90 odstotkov vseh primerov malarije po svetu, uspelo občutno zmanjšati breme te smrtonosne bolezni. V 20 letih naj bi se število smrtnih žrtev zmanjšalo za 40 odstotkov, v tem času naj bi tako preprečili 1,5 milijarde novih primerov bolezni in 7,6 milijona smrti. Toda napredek, opozarjajo v poročilu, se upočasnjuje zlasti zaradi vse manjše finančne podpore, položaj pa je dodatno zaostrila tudi koronavirusna epidemija. Že samo 10-odstotni padec finančne podpore pri zagotavljanju sredstev za preventivo in zdravila bi v državah obsaharske Afrike pomenil dodatnih 19.000 smrti zaradi malarije več na leto.




















































 2. sv
2. sv








Komentarji so trenutno privzeto izklopljeni. V nastavitvah si jih lahko omogočite. Za prikaz možnosti nastavitev kliknite na ikono vašega profila v zgornjem desnem kotu zaslona.
Prikaži komentarje