

Metode naslednje generacije določanja nukleotidnega zaporedja imenujemo metode, ki so se razvile v zadnjem desetletju ter omogočajo hitro in poceni določanje zaporedja celotnega genoma (celoten genski zapis v eni celici) ali njegovih delov. Z njihovim razvojem se odpirajo fascinantne možnosti na področju naravoslovja, posebej na področju personalizirane medicine, prepoznavanju vzrokov bolezni, razvoju novih zdravil in diagnostiki, na področju analize celotnega transkriptoma (analiza izražanja vseh genov v celici naenkrat), analize uravnavanja izražanja genov in analize različnih RNK-molekul, za katere danes vemo, da imajo zelo pomembno vlogo. S starejšimi metodami določanja zaporedja DNK je bilo določanje zaporedja človeškega genoma ogromen projekt, ki je zahteval milijone dolarjev, sodelovanje več inštitucij in več let časa. Danes lahko to delo opravimo v nekaj tednih ali celo dnevih znotraj enega laboratorija.
Med najnovejšimi načini sekvenciranja DNK je posebej zanimiva tehnologija nanopor (luknjic s premerom nekaj nanometrov), ki ji je uspelo preseči glavno pomanjkljivost drugih sorodnih metod – dolžino odčitkov. Tehnologijo je do zdaj uspelo najdlje razviti angleškemu podjetju Oxford Nanopore Technologies. Z novo tehnologijo tako lahko določimo zaporedje zelo dolgih delov DNK naenkrat, kar olajša analizo podatkov. Najdaljši del DNK, ki so ga uspešno prebrali, je bil dolg 155 000 nukleotidov. Naprave za zdaj še ni na trgu, jo pa preizkuša nekaj sto laboratorijev po svetu, med njimi tudi Laboratorij za molekularno biologijo in nanobiotehnologijo na Kemijskem Inštitutu v Ljubljani pod vodstvom prof. dr. Gregorja Anderluha. Skupina prof. Anderluha v sodelovanju s podjetjem Oxford Nanopore Technologies raziskuje naravne proteinske nanopore, ki bi bile primerne za podobne aplikacije. Tovrstne pristope hitrega določanja zaporedij pa bodo uporabili tudi pri raziskavah molekulskih interakcij. Zanimivo je, da je ideja za tehnologijo, ki stoji za napravo, stara že 20 let, naprava pa je v testni uporabi šele 2 leti.
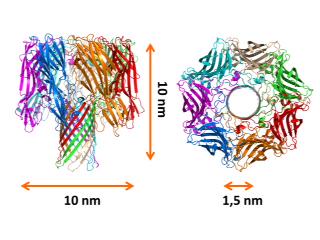
Vsaka celica je obdana z membrano, v kateri je veliko različnih proteinov – od receptorjev do proteinov, ki membrani dajajo trdnost, in transportnih proteinov, ki omogočajo prehod različnih molekul v celico in iz nje. Nekateri od teh proteinov v membrani tvorijo pore. Raziskovalci so izkoristili znanje o strukturi in lastnostih membranske pore naravnega toksina, alfa toksin, ki ga izloča bakterija Staphylococcus aureus, ter razvili poseben sistem v velikosti USB-ključka, ki omogoča določanje zaporedja nukleotidov v molekuli DNK, RNK in miRNK ter raziskovanje interakcij med proteini, kar omogoča povsem neposreden mehanizem delovanja naprave (brez označevanja in pomnoževanja DNK, ki je potrebno pri drugih tehnologijah). Naprava je sestavljena iz umetne membrane s proteinskimi porami. Umetna membrana s površino manj kot 1 cm2 vsebuje okoli 500 proteinskih por, skozi katere v električnem polju lahko potujejo enoverižne molekule DNK. DNK izoliramo iz tkiva ali organizma, ki nas zanima (tehnologija nanopor omogoča tudi sekvenciranje DNK iz kompleksnih vzorcev, npr. krvi in različnih vodnih virov), jo razrežemo in na konce pritrdimo posebne adapterje, ki povežejo molekulo DNK s poro na čipu. Medtem ko molekula DNK prehaja skozi poro, vsaka dušikova baza na vijačnici (Adenin, Timin, Citozin, Gvanin – osnovne enote, iz katerih je sestavljena DNK) zaradi različne velikosti povzroči specifično spremembo v električnem toku skozi poro, ki jo računalniški program zazna in dekodira. Za določanje zaporedja DNK sta tako potrebna le prenosni računalnik in omenjena naprava velikosti USB-ključa. S to tehnologijo naj bi bilo s paralelizacijo in uporabo več takšnih aparatur določanje zaporedja celotnega človeškega genoma možno v 15 minutah za manj kot tisoč evrov. Naprave za določanje zaporedja genomov v obliki USB-ključka bodo širše uporabne, tudi v drugih vedah, npr. v epidemiologiji, antropologiji, botaniki in bodo omogočale tudi delo na terenu in v zahtevnejših razmerah.
Pri določanju zaporedja DNK nikoli ne določamo zaporedja celotne izredno dolge molekule DNK, ker nobena do zdaj razvita tehnologija tega ne omogoča. Pri večini postopkov DNK najprej razrežemo na naključnih mestih ter nato določimo zaporedje odsekom, dolgim do 1000 baznih parov. Ker analiziramo mešanico zaporedij, kjer so deli DNK zastopani večkrat s sekvencami različnih dolžin, lahko nato prebrana zaporedja na osnovi prekrivanja s pomočjo rečunalniškega programa sestavimo v celotno zaporedje genoma. Pri tem načinu so težava predvsem regulatorna območja DNK (območja, kamor se vežejo različni proteini, ki sprožijo ali zavrejo izražanje genov), ki so sestavljena iz ponavljajočih se zaporedij (npr. ACGTCG ACGTCG, kjer se to zaporedje lahko ponovi tudi več stokrat). V človeškem genomu naj bi kar 43 % zapisa predstavljala ponavljajoča se zaporedja. Ta zaporedja sicer lahko sekvenciramo, vendar imamo potem težave pri sestavljanju v celotno zaporedje genoma.
Z novejšimi že obstoječimi metodami in prihajajočimi novimi tehnologijami branja nukleotidnega zaporedja lahko računamo na veliko uspešnejše, hitrejše in cenejše določanje zaporedij DNK, kar bi pomenilo veliko revolucijo za biološke vede. V naslednjih letih načrtujejo določanje zaporedja 1000 človeških genomov, s čimer bi zajeli večino razlik med posamezniki ter ustvarili referenčno zaporedje človeškega genoma, ki bi ga nato uporabljali pri genetskih analizah.
Mojca Jež, univ. dipl. biotehnologinja




















































 2. sv
2. sv













Komentarji so trenutno privzeto izklopljeni. V nastavitvah si jih lahko omogočite. Za prikaz možnosti nastavitev kliknite na ikono vašega profila v zgornjem desnem kotu zaslona.
Prikaži komentarje